En désactivant un frein naturel à la synthèse des acides gras, les chercheurs du BIAM ont réussi à multiplier par cinq la teneur en huile des microalgues. Une avancée considérable pour l’optimisation des bioénergies, qui ouvre la voie à une plus grande efficacité de production durable.
Les acides gras jouent un rôle essentiels dans la structure des membranes cellulaires, dans le stockage du carbone et la signalisation. En utilisant les outils d’édition du génome Crispr (voir encadré), les chercheurs du BIAM ont démontré qu’il était possible pour les microalgues de produire cinq fois plus d’acide gras, grâce à la désactivation d’un régulateur naturel qui en limitait la production. Mieux comprendre comment la production d’acides gras est régulée dans le chloroplaste (petite usine présente dans les cellules des plantes, où a lieu la photosynthèse) ouvre la voie à de nouvelles stratégies pour optimiser cette production chez les microalgues.
Une première étape de synthèse des acides gras soumise à une régulation aux multiples facettes
Il est bien connu qu’avec l’aide de l’énergie lumineuse, la photosynthèse transforme le carbone issu du CO2 atmosphérique en carbone organique et en énergie chimique. Les cellules doivent alors répartir correctement leurs ressources pour fabriquer différents composants essentiels à leur fonctionnement comme les protéines, les sucres ou les acides gras. Un déséquilibre dans cette répartition, qu’il s’agisse d’un déficit ou d’un excès, pourrait compromettre l’aptitude et la survie de la cellule.
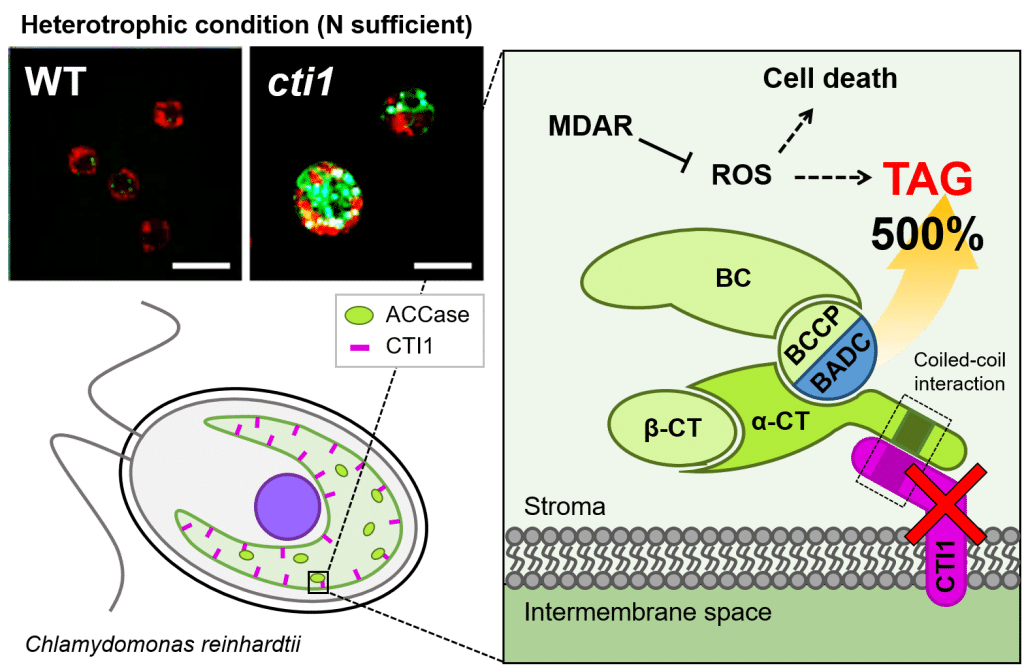
L’inactivation de CTI1, un régulateur négatif de la synthèse des acides gras, a permis de multiplier par cinq la teneur en huile cellulaire.
La première étape de la synthèse de novo1 des acides gras dans le chloroplaste repose sur l’action d’une enzyme clé dans ce processus, l’acétyl-CoA carboxylase (ACCase). Toutefois, son activité n’est pas constante : elle est finement régulée par divers signaux qui l’activent ou l’inhibent, permettant ainsi d’ajuster précisément l’utilisation du carbone et de l’énergie dans la synthèse des acides gras.
Identification d’un régulateur négatif clé de la synthèse de novo des acides gras et son utilisation pour augmenter la teneur en lipides
Dans le cadre d’une collaboration internationale, les chercheurs du BIAM ont découvert chez Chlamydomonas une protéine semblable à Carboxyltransférase Interactor 1 (CTI1), déjà identifiée chez d’autres espèces. La carboxyltransférase est une enzyme essentielle à la fabrication des acides gras, car elle intervient dès les premières étapes du processus. L’homologue identifié, nommé CrCTI1, interagit avec une sous-unité du complexe ACCase et agit comme un frein naturel à la production d’acides gras.
Grâce aux outils avancés d’édition du génome, l’équipe a ainsi démontré que la suppression du gène CrCTI1 dans les cellules d’algues entraine une multiplication par cinq de la teneur en huile, sans altérer la croissance cellulaire.
Contrairement aux plantes, où l’accumulation de lipides dépend principalement de la lumière, le phénotype de l’huile des mutants crcti1 est principalement influencé par des conditions de croissance trophique. En cultivant les cellules dans des conditions hétérotrophiques (où elles se nourrissent de sources de carbone externes plutôt que la lumière), les scientifiques ont observé une fonction cruciale de CrCTI1 dans la régulation de l’équilibre entre l’accumulation de lipides et la croissance cellulaire. Les analyses cellulaires montrent que CrCTI1 joue un rôle essentiel dans la gestion du carbone. Il permet aux cellules de s’adapter à la quantité de carbone disponible en contrôlant le métabolisme du carbone, les antioxydants et l’oxydation des graisses.
Ces résultats s’inscrivent dans la continuité des recherches sur la régulation du métabolisme lipidique et renforcent les perspectives d’applications biotechnologiques. En approfondissant la compréhension des mécanismes de contrôle de la synthèse des acides gras il est désormais envisageable de quintupler leur production, augmentant ainsi leur potentiel en tant que source d’énergie renouvelable.
L’édition génomique, un travail de dentelle
Les outils d’édition du génome CRISPR sont comme des « ciseaux génétiques »ultra-précis, i. Ils permettent de modifier l’ADN d’un organisme en coupant une séquence spécifique pour la supprimer l’ajouter ou la corriger. Il est à noter que ces ajustements ciblés reposent sur des mécanismes naturels déjà présents dans les cellules et offrent une maîtrise sans précédent sur l’édition du génome.
1 La synthèse de novo des acides gras désigne le processus par lequel les cellules fabriquent des acides gras à partir despetites molécules comme l’acétyl-CoA.
Auteurs :
Zhongze Li1, Minjae Kim1, 2, Jose Roberto da Silva Nascimento3, Bertrand Legeret1, Gabriel Lemes Jorge3, Marie Bertrand1, Fred Beisson1, Jay J Thelen3*, Yonghua Li-Beisson1*
Collaboration :
1Aix-Marseille Université, CEA, CNRS, Institute of Biosciences and Biotechnologies of Aix-Marseille, UMR 7265, CEA Cadarache, Saint-Paul-lez Durance F-13108, France
2Library of Marine Samples, Korea Institute of Ocean Science & Technology, Geoje 53201, Republic of Korea
3Department of Biochemistry and Interdisciplinary Plant Group, University of Missouri, Christopher S. Bond Life Sciences Center, Columbia, Missouri 65211, United States
Références
Plant Biotechnology Journal. DOI 10.1111/pbi.14581